対象となるがん
尿路上皮癌
使用される新薬(治験薬)
Erdafitinib(抗がん剤)
Erdafitinib(抗がん剤)について
今回、使用するお薬はFGFR(線維芽細胞増殖因子受容体)ファミリーを標的とする分子標的薬です。
FGFRは正常細胞にも存在している受容体で、人間の体内にもともとあるFGFという増殖因子と結合すると、活性化されます。活性化されたFGFRは細胞の増殖や成長を刺激します。
一方、一部の方のがん細胞にもこのFGFRは発現しており、がん細胞の増殖、生存、転移、腫瘍内での新しい血管の形成に重要な役割を担っていることがわかっています。
FGFRの活性化を妨げ、がん細胞の増殖や成長を妨げる効果が期待されているのが今回の治験薬です。
本治験薬は1日1回の内服薬です。米国では既に「FGFR遺伝子異常陽性の進行性・再発の尿路上皮がん」に対して承認されています。
実施方法(治験のデザイン)
第Ⅲ相 ランダム化比較試験(国際共同治験)
治験デザインの概略
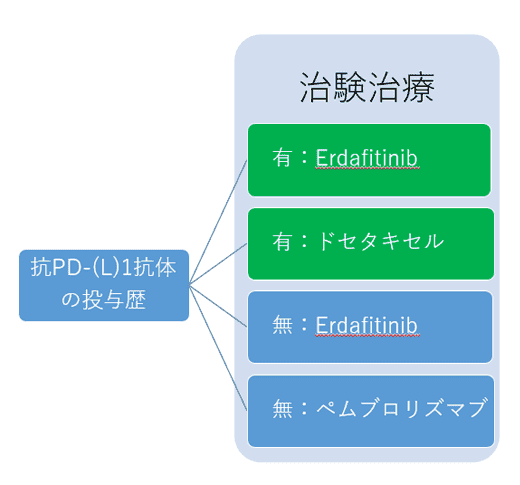
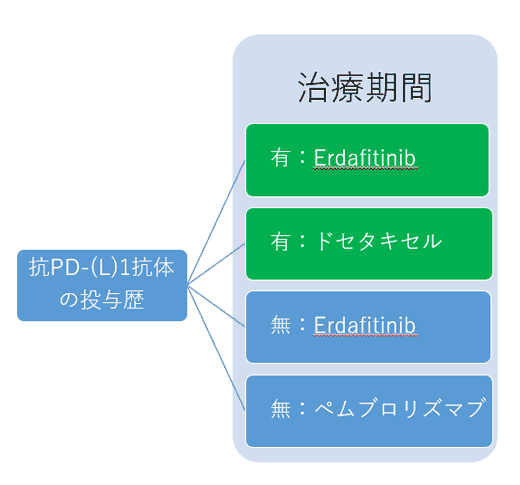
試験の目的
特定のFGFR異常を有し、以前に1種類若しくは2 種類の治療[少なくともこのうち1種類は抗PD-(L)1 抗体を含む(コホート1)]、又は抗PD-(L)1 抗体を含まない1 種類の治療を受けるも進行が見られた進行性尿路上皮癌患者様を対象に、erdafitinibと化学療法剤又はペムブロリズマブの有効性を比較評価すること。
治験に参加できる方(患者選択基準)
- 18歳以上の方
- 尿路上皮がん(膀胱がん、腎盂がん、尿管がん)と診断されている方
- お薬による治療を行ったことがある方
- FGFR遺伝子変異が陽性である方(試験に参加された際に検査で確認します)
※この他にも細かな条件があります。
治験責任医師
常森 寛行
